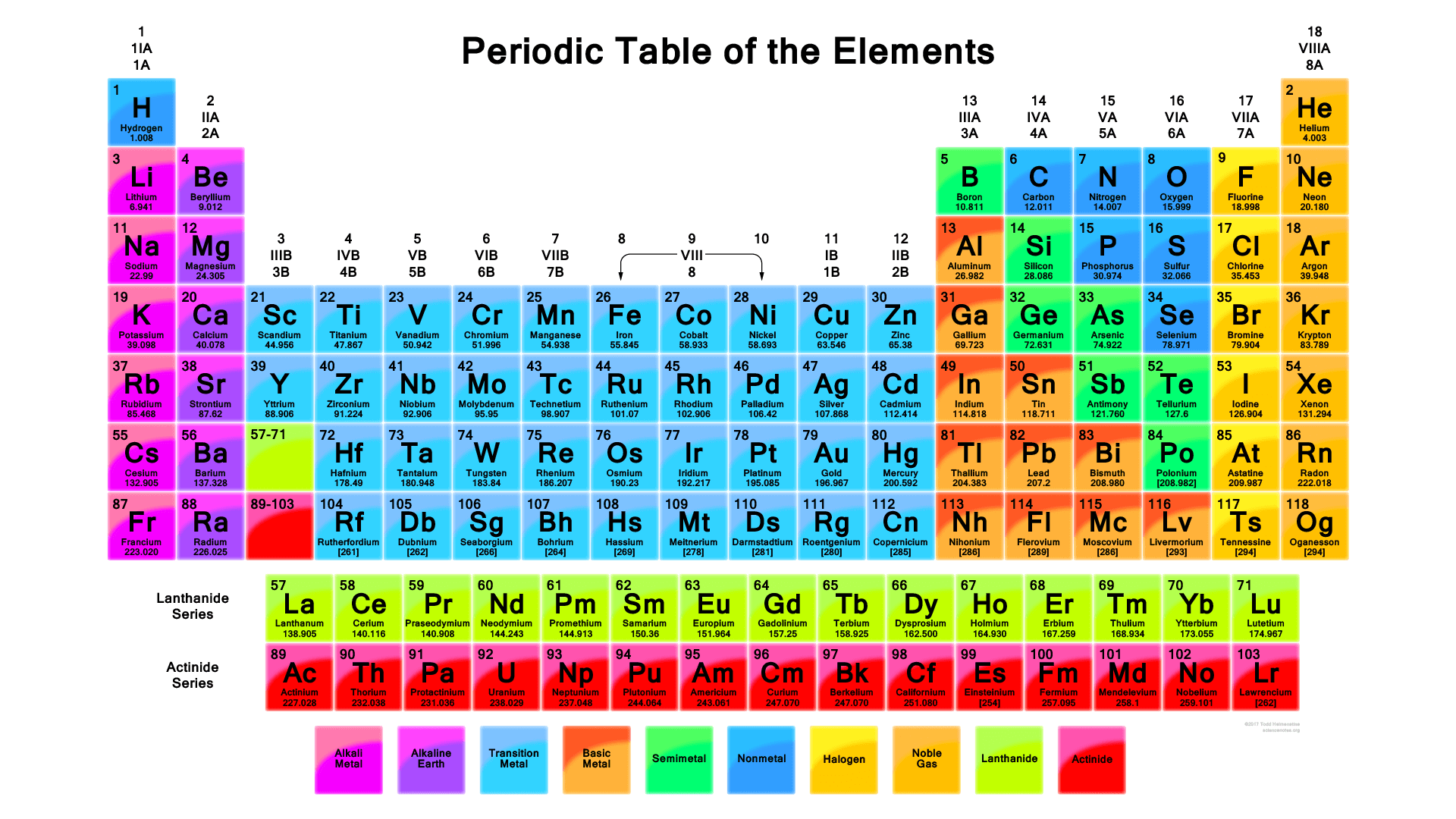
Tabel periodik unsur menghiasi halaman setiap buku pelajaran kimia dan dinding setiap laboratorium sekolah menengah. Bagan sederhana ini merupakan ”kamus” bagi setiap kimiawan untuk menjelaskan unsur-unsur yang membentuk segala sesuatu di alam semesta dalam kuantitas yang terukur, seperti nomor atom dan massa atom.
Tabel periodik dibentuk dengan cara mengelompokkan berdasarkan pada kesamaan dan perbedaan antar unsur. Unsur-unsur disusun ke dalam golongan secara tegak (vertikal) dan horizontal. Unsur-unsur dalam satu golongan memiliki sifat-sifat kimia dan fisika yang serupa.
Perkembangan Sistem Periodik Unsur
1. Tabel Periodik Unsur Mendeleyev
Legenda menyebutkan bahwa Mendeleyev mendapatkan gagasan tabel periodik ketika dia sedang bermain sebuah permainan kartu yang bernama solitaire. Namun, hanya terdapat sedikit bukti sejarah yang menyokong cerita ini.
Jelaslah bahwa Mendeleyev menyusun tabel itu menggunakan daftar massa atom yang dihasilkan pada tahun 1860 di pertemuan sains di Karlsruhe, Jerman.
Massa atom adalah jumlah proton dan neutron di dalam inti atom. Mendeleyev percaya bahwa massa atom merupakan sifat unsur yang paling penting, walaupun sekarang kita mengetahui bahwa unsur-unsur ditetapkan berdasarkan nomor atomnya.
Kemungkinan besar Mendeleyev menghasilkan tabel periodik ketika dia sedang menulis sebuah buku pelajaran yang berjudul The Principles of Chemistry atau Prinsip-Prinsip Kimia (1868-1870). Di dalam bukunya, Mendeleyev menggolongkan unsur-unsur berdasarkan kesamaan sifat-sifat fisika dan kimia.
Sebagai contoh, dia menggolongkan halogen (unsur-unsur Golongan 17) dalam satu bab dan logam-logam alkali pada bab yang lain.
Mendeleyev menggolongkan unsur-unsur yang bervalensi sama. Valensi adalah ukuran jumlah ikatan yang dapat dibentuk oleh suatu atom dengan atom lain. Valensi ditentukan oleh jumlah elektron pada kulit elektron terluar suatu atom.
Atom berbagi atau memberikan elektron-elektron terluarnya untuk membentuk ikatan kimia dengan atom-atom lainnya. Unsur-unsur halogen memiliki sifat yang sama karena semuanya memiliki tujuh elektron pada kulit elektron terluar dan semua siap menerima satu elektron untuk membentuk ikatan dengan unsur-unsur lainnya.
Sebaliknya, logam-logam alkali memiliki kesamaan sifat-sifat fisika dan kimia karena logamlogam alkali hanya memiliki satu elektron di kulit elektron terluarnya dan siap memberikan elektron untuk membentuk ikatan dengan unsur-unsur lain.
Saat Mendeleyev mencoba menggolongkan unsur-unsur yang sama, suatu pola muncul. Dia menyusun 61 unsur yang telah diketahui dalam suatu bagan berdasarkan kenaikan massa atom. Hasil karya Mendeleyev memungkinkan para kimiawan mencirikan golongan unsur yang memiliki sifat-sifat kimia yang sama.

Pada tabel tersebut, Mendeleyev menemukan bahwa unsur-unsur dengan valensi sama muncul pada kolom yang sama. Mendeleyev telah memolakan struktur dasar tabel periodik. Dia mempublikasikan penemuannya pada tahun 1869 dan menghasilkan tabel yang telah diperbaiki pada tahun 1871 yang menempatkan unsur-unsur ke dalam delapan golongan.
Dimitry Ivanovich Mendeleyev lahir di Tobol’sk, Siberia pada tanggal 8 Februari 1834. Sedari usia muda, Dia terlihat bakat ilmuwan. Ibunya mencoba mencarikan universitas, tetapi Mendeleyev tidak diterima di Universitas Moscow dan Universitas St. Petersburg di Rusia.
Akhirnya, pada tahun 1850 Dia mendaftarkan diri mengikuti pelatihan guru sains di Institut St. Petersburg dan lulus dengan predikat luar biasa. Pada tahun 1855, dia bekerja sebagai guru sains di Simferopol dekat Laut Hitam.
Setahun kemudian, dia kembali ke St. Petersburg untuk menyelesaikan gelar master. Tahun 1859, Dia melakukan perjalanan ke luar negeri untuk bekerja di berbagai laboratorium di Eropa.
Pada kepulangannya tahun 1861, Mendeleyev memusatkan pada karir akademik dan akhirnya menjadi profesor kimia di Universitas St. Petersburg. Tahun 1869, dia mempublikasikan tabel periodik versi pertamanya. Tahun-tahun terakhirnya dia habiskan sebagai direktur biro metrologi di St. Petersburg.
Mendeleyev menerima banyak penghargaan dari universitas-universitas seluruh dunia. Tahun 1906, dia menerima Hadiah Nobel di bidang kimia. Dia meninggal di St. Petersburg pada tahun 1907.
Keunggulan Tabel Periodik Unsur Mendeleyev
Salah satu pencapaian terbesar Mendeleyev adalah menempatkan unsur-unsur pada tempat yang baru di dalam bagan meskipun mengacaukan urutan berdasarkan massa atom.
Dengan cara ini, dia mempertahankan urutan unsur berdasarkan valensi. Barangkali, pencapaian terbesar adalah menggambarkan unsur-unsur yang belum ditemukan. Mendeleyev yakin dengan urutan alami pada tabel periodik.
Namun, di tabelnya masih banyak tempat yang kosong dan Mendeleyev beralasan bahwa tempat yang kosong tersebut pasti berisi unsur-unsur yang belum ditemukan. Dia bahkan memperkirakan sifat-sifat fisika dan kimia unsur-unsur yang belum ditemukan itu.
Salah satu tempat yang kosong pada tabel Mendeleyev ada di bawah aluminium sehingga ia menamakannya ekaaluminium (eka berasal dari bahasa Sansekerta yang berarti “satu” dan ekaaluminium di dalam tabel periodik berada satu tempat setelah aluminium).
Unsur ini ditemukan oleh ilmuwan Prancis Paul-Emile Lecoq de Boisbaudran (1838-1912) pada tahun 1875. Dia menyebutnya gallium untuk menghormati negaranya (Gallia merupakan nama Latin untuk Prancis).
Pada tahun 1879, kimiawan Swedia Lars Frederick Nilson (1840-1899) menemukan unsur yang oleh Mendeleyev disebut sebagai eka-boron. Nilson menamai unsur tersebut skandium sebagai penghormatannya pada Skandinavia.
Pada tahun 1886, kimiawan Jerman Clemens Winkler (18381904) menemukan eka-silikon Mendeleyev. Winkler menamainya germanium sebagai penghormatannya pada Jerman. Pada semua kasus, sifat-sifat unsur-unsur baru cocok dengan perkiraan Mendeleyev.
Penemuan Gas Mulia
Pada tahun 1895, kimiawan Inggris John William Strutt, Lord Rayleigh (1842-1919), dan kimiawan Skotlandia William Ramsay (1852-1916) mencirikan suatu gas yang mereka sebut argon. Unsur baru tersebut tampaknya tidak cocok untuk diletakkan di dalam tabel periodik Mendeleyev.
Ramsay berpendapat bahwa gas-gas yang sama dengan argon pasti ada dan merencanakan untuk mencoba menemukannya. Pada tahun 1895, dia mendapatkan helium. Pada tahun 1898 dia mengadakan penelitian lebih lanjut bersama kimiawan Inggris Morris Travers.
Bersama-sama mereka mencirikan neon, kripton, dan xenon. Gas-gas mulia sulit bereaksi dengan unsur-unsur lain, sehingga merupakan golongan unsur-unsur yang ditemukan paling akhir dan golongan yang paling terakhir ditambahkan pada tabel periodik.
Empat tahun kemudian, Mendeleyev memperbaiki tabel periodiknya. Dia meletakkan kelompok baru gas itu pada satu golongan di bagian ujung tabel periodik. Semula para kimiawan menamai golongan unsur ini sebagai “gas lembam” karena gas-gas itu tidak dapat bereaksi dengan unsur-unsur lain. Sekarang, gas lembam disebut gas mulia karena gas-gas itu dapat bereaksi pada keadaan tertentu.
2. Tabel Periodik Moseley
Pada tahun 1911, fisikawan Selandia Baru kelahiran Inggris Ernest Rutherford (1871-1937) melakukan sebuah penelitian penting. Penelitian ini mengungkapkan bahwa pusat atom terdiri atas sebuah inti padat yang bermuatan positif.
Dua tahun setelah penemuan Rutherford, fisikawan Inggris Henry Moseley (1887-1915) menggunakan sebuah alat yang disebut pistol elektron untuk menembakkan elektron-elektron pada atom-atom dari berbagai macam unsur. Dia mendapati bahwa unsur-unsur itu memancarkan sinar-X (radiasi berenergi tinggi dengan panjang gelombang pendek).
Sinar-X ini memiliki sifat-sifat yang tergantung pada jumlah proton di dalam inti. Moseley menulis nomor proton (sekarang disebut nomor atom) dari banyak macam unsur. Kemudian, dia membuat sebuah bagan semua unsur yang telah diketahui berdasarkan peningkatan nomor proton.

Mengikuti langkah Mendeleyev, Moseley juga meninggalkan kekosongan pada daftar, memperkirakan keberadaan dua unsur baru.
Unsur-unsur yang belum ditemukan ini nantinya ditemukan dan diberi nama teknetium dan prometium. Moseley juga memperbaiki beberapa kesalahan yang berhubungan dengan tabel yang disusun berdasarkan massa atom.
Mengapa Tabel Periodik disusun bukan berdasarkan massa atom?
Massa atom adalah ukuran banyaknya proton dan neutron di dalam inti sebuah atom. Atom-atom suatu unsur selalu memiliki jumlah proton yang sama tetapi bisa memiliki jumlah neutron yang berbeda. Jenis atom yang berbeda ini disebut isotop.
Nomor atom adalah sifat dasar yang membuat tabel periodik menjadi terorganisasi dengan sangat baik, bukan massa atom. Untung bagi Mendeleyev yang tidak mengetahui tentang proton dan neutron, massa atom dan nomor atom meningkat dengan perbandingan yang hampir sama.
Suatu isotop teknetium biasanya digunakan pada beberapa alat pemindai yang memungkinkan dokter dapat melihat bagian dalam tubuh pasien. Hasil pindaian ini memperlihatkan seseorang yang menderita Alzheimer. Bagian terputus pada cincin merah (kiri agak bawah) menujukkan daerah otak yang mengalami penurunan.
3. Tabel Periodik Modern

Perubahan besar terakhir pada tabel periodik terjadi pada pertengahan abad ke-20. Fisikawan Amerika Glenn Seaborg (1912-1999) dan rekannya menemukan 11 unsur baru dengan nomor atom lebih besar daripada nomor atom uranium (nomor atom 92).
Seaborg menyusun ulang tabel periodik untuk menampung unsur-unsur baru tersebut.
Membaca Tabel Periodik Unsur
Tabel periodik menyusun unsur-unsur berdasarkan peningkatan nomor atom. Baris disebut periode dan kolom disebut golongan. Umumnya, unsur-unsur pada kolom yang sama memiliki sifat kimia yang mirip.
Susunan elektron di dalam atom-atom unsur-unsur menentukan struktur tabel periodik itu sendiri.

Gambaran klasik tabel periodik tersebut menyusun unsur-unsur ke dalam 18 golongan yang disusun dalam 7 baris. Baris disusun berdasarkan peningkatan nomor atom dari kiri ke kanan.
Semua anggota dalam satu golongan menunjukkan sifat-sifat sejenis dalam hal bagaimana mereka bereaksi secara kimia dengan golongan-golongan lain di dalam tabel.
Semua gas kecuali hidrogen terletak pada bagian paling kanan dan semua logam terletak di kiri dan tengah. Logam merupakan bagian terbesar dari unsur-unsur. Kebanyakan unsur radioaktif ada pada golongan aktinida.

Salah satu sumber utama unsur berilium adalah mineral yang tersusun atas aluminium, silikon, dan oksigen. Salah satu bentuk kristalnya disebut akuamarin yang dipotong menjadi batu permata biru pucat yang berkilauan. Batu Zamrud adalah bentuk lain dari mineral ini.
Dasar Penyusunan Unsur dalam Tabel Periodik
Nomor atom suatu unsur adalah jumlah proton di dalam inti satu atom unsur itu. Sebuah atom hidrogen selalu memiliki satu proton di dalam intinya. Nomor atomnya 1 sehingga hidrogen menempati tempat pertama di dalam tabel periodik.
Sebuah atom helium selalu memiliki dua proton di dalam inti. Nomor atomnya 2, sehingga helium menempati tempat kedua di dalam tabel periodik setelah hidrogen. Sebuah atom uranium selalu memiliki 92 proton, sehingga uranium menempati urutan ke 92.
Penyusunan unsur berdasarkan nomor atom menghilangkan masalah yang dihadapi Mendeleyev ketika menyusun unsur berdasarkan massa atom. Dari kiri ke kanan di sepanjang sebuah baris pada tabel periodik, nomor atom naik satu satuan setiap unsurnya.
Unsur-unsur yang berada di baris yang lebih bawah memiliki nomor atom lebih besar daripada unsur-unsur di atasnya. Kimiawan yakin bahwa tidak ada nomor atom dan unsur yang kurang.
Informasi yang Diperoleh dari Tabel Periodik Unsur
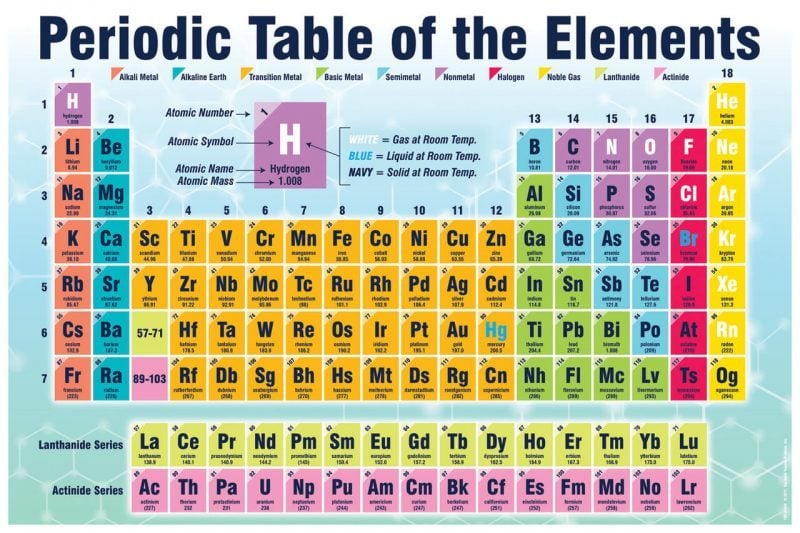
Setiap kotak pada tabel periodik mewakili satu unsur. Kotak tersebut harus menunjukkan nomor atom, nama, dan simbol kimia unsur. Di samping itu, tidak ada peraturan yang mengikat.
Massa atom biasanya dimasukkan karena mencerminkan sejarah tabel periodik. Beberapa versi mungkin memiliki sampai 20 data untuk setiap unsurnya. Sebagai contoh, termasuk susunan elektron dan apakah biasanya unsur itu berbentuk padat, cair, atau gas pada kondisi suhu dan tekanan baku.
Pada kebanyakan tabel modern, unsur-unsur juga diberi arsiran atau warna sesuai dengan jenisnya dan menunjukkan mana yang logam, non logam, atau metaloid. Tabel-tabel lainnya memiliki warna khas untuk setiap golongan unsur.
Sebagai contoh, satu warna untuk logam alkali satu warna untuk halogen dan lain-lain. Tidak semua tabel periodik disusun dalam baris atau kolom. Beberapa disusun dalam spiral atau dalam bentuk-bentuk yang mewakili hubungan antara sifat-sifat kimia unsur.
1. Baris Disebut Periode
Tujuh baris utama pada tabel periodik disebut periode. Hidrogen dan helium menyusun periode 1. Berikutnya dua periode pendek yang terdiri atas delapan unsur. Periode 2 dimulai dengan litium (nomor atom 3) dan diakhiri dengan neon (10).

Saat berpindah dari satu unsur ke unsur lain di sepanjang baris, sifat kimianya berubah dari logam (Li dan Be) ke metaloid (B), sampai non logam (C), dan akhirnya gas (N,O, F, dan Ne).
Periode 3 dimulai dengan natrium (11) dan diakhiri dengan argon (18). Terdapat dua periode panjang, masing-masing periode berisi 18 unsur. Periode 4 dimulai dengan kalium (19) dan diakhiri dengan kripton (36). Periode 5 dimulai dengan rubidium (37) dan diakhiri dengan xenon (54).
Sebagian unsur pada periode panjang 4 dan 5 disebut logam transisi. Pada periode 4, logam transisi dimulai dengan skandium (21) dan diakhiri dengan zink (30). Pada periode 5, logam transisi dimulai dengan itrium dan diakhiri dengan kadmium (48).
Periode 6 merupakan baris yang sangat panjang, berisi 32 unsur, dimulai dengan sesium (55) dan diakhiri dengan radon (86). Pada tabel periodik yang paling modern, unsur-unsur pada Periode 6 dikurangi sampai menjadi 18 unsur dengan memindahkan 14 unsur yang disebut lantanida ke bagian bawah tabel.
Dengan cara ini, tabel tidak hanya muat untuk halaman buku berukuran normal, tetapi juga memungkinkan untuk menempatkan unsur-unsur dengan valensi sama pada kolom yang sama. (Valensi tergantung pada jumlah elektron pada kulit terluar dan menentukan reaktivitas unsur).
Jadi, logam transisi pada Periode 6 diakhiri dengan merkurium (80) yang terletak langsung di bawah kadmium, logam transisi terakhir ada di Periode 5.
Periode 7 merupakan baris yang tidak lengkap, diakhiri dengan unsur buatan 116 (unsur terakhir yang dikenali secara resmi). Unsur-unsur buatan tidak ada di alam tetapi harus di buat di laboratorium oleh ilmuwan.
Periode 7 merupakan periode sangat panjang lainnya, dengan 32 unsur yang akan lengkap ketika unsur 118 ditemukan. Periode 7 juga diperpendek dengan memindahkan 14 unsur yang disebut aktinida ke bagian bawah tabel.
2. Kolom Disebut Golongan
Unsur-unsur yang memiliki jumlah elektron yang sama pada kulit elektron terluarnya biasanya terdapat pada kolom yang disebut golongan (kanan). Para kimiawan meletakkan hidrogen pada bagian teratas golongan 1, tetapi hidrogen tidak benar-benar menjadi bagian dari golongan itu.
Sebenarnya Golongan 1 dimulai dengan litium (3) dan diakhiri dengan fransium (87). Tidak seperti hidrogen, unsur-unsur Golongan 1 merupakan unsur-unsur logam yang lunak dan kuat. Semua unsurnya bereaksi dengan air membentuk larutan alkali. Untuk alasan inilah unsur-unsur Golongan 1 disebut logam alkali.

Pada sebagian besar versi tabel periodik, hidrogen diletakkan di atas logam alkali di Golongan 1 pada bagian kiri atas tabel periodik. Namun, ada suatu masalah dengannya karena hidrogen adalah gas dan semua unsur Golongan 1 merupakan logam.
Pada versi tabel periodik lainnya, hidrogen dapat ditemukan di atas halogen pada Golongan 17. Kadang, hidrogen muncul di kedua golongan tersebut dan kadang-kadang diletakkan terapung dengan bebas di bagian paling atas tabel. Faktanya, hidrogen merupakan unsur unik yang tidak seorang pun tahu tempatnya.
Unsur-unsur Golongan 2 dimulai dengan berilium (4) dan diakhiri dengan radium (88). Unsur-unsur Golongan 2 dikenal sebagai logam alkali tanah. Logam-logam ini juga bereaksi dengan air membentuk larutan alkali.
Kata tanah berasal dari istilah kuno yang digunakan untuk menggambarkan senyawa-senyawa yang terbentuk ketika logam-logam Golongan 2 direaksikan dengan oksigen.
Golongan 3 sampai 12 terdiri atas logam transisi di tengah-tengah tabel periodik dan logam tanah-langka pada bagian bawah tabel. Sifat kimia logam transisi lebih sulit diramalkan daripada sifat kimia logam alkali dan logam alkali tanah.
Beberapa logam transisi, seperti kobalt (27) dan besi (26) membentuk banyak senyawa berwarna. Lainnya seperti emas (79) dan platina (78) hampir tidak bereaksi sama sekali dan dapat ditemukan sebagai logam murni di alam.
Golongan 13, 14, 15, dan 16 membentuk golongan unsur-unsur yang tampaknya tidak berhubungan secara jelas dengan golongan-golongan sebelumnya. Metaloid (unsur-unsur mirip logam) seperti boron (6) dan silikon (14) dan banyak padatan nonlogam seperti fosforus (15) dan sulfur (16) terdapat di Golongan 13 sampai 16.
Unsur-unsur halogen menyusun Golongan 17. Golongan ini dimulai dengan fluorin (9) dan diakhiri dengan astatin (85). Semua unsur halogen reaktif, fluorin merupakan unsur yang paling reaktif di antara unsur-unsur lainnya.
Unsur-unsur Golongan 18 dimulai dengan helium (2) dan diakhiri dengan radon (86). Gas-gas ini belum ditemukan ketika tabel asli Mendeleyev dipublikasikan pada tahun 1869. Mendeleyev menambahkannya di akhir tabel yang telah ia perbaiki pada tahun 1902.
Unsur-unsur Golongan 18 tidak bereaksi dengan banyak unsur lainnya. Oleh karena itu, unsur-unsur ini dikenal sebagai gas mulia atau lembam.
3. Konvensi Penomoran
Dari atas sampai bawah tabel periodik, periode-periode (baris-baris) diberi nomor dari 1 sampai 7. Penomoran golongan lebih sulit. Ada tiga sistem dalam menomori golongan. Sistem pertama menggunakan angka Romawi (I, II, III, IV, V, dan seterusnya).
Sistem kedua menggunakan kombinasi angka Romawi dan huruf A dan B. Pada tahun 1985, International Union of Pure and Applied Chemistry (IUPAC) mengganti angka Romawi dan huruf.
Sistem terbaru menggunakan angka Arab 1 sampai 18, dimulai dengan logam alkali (Golongan 1) dan diakhiri dengan gas mulia (Golongan 18). Kamu mungkin masih melihat sistem lama yang digunakan pada buku-buku pelajaran karena banyak kimiawan tidak ingin mengubah penomoran angka Romawi.
Lambang Kimia
Lambang kimia adalah cara singkat menulis nama unsur. Lambang kimia digunakan dalam penulisan persamaan kimia. Lambang itu sendiri terdiri atas satu atau dua huruf. Biasanya, lambang kimia merupakan huruf pertama nama umum unsurnya sehingga hidrogen ditulis ”H” dan boron ”B”.
Kadang, lambang kimia merupakan huruf pertama nama Latin unsur tersebut. Sebagai contoh, kalium ditulis ”K”. Tak dapat dielakkan, nama beberapa unsur dimulai dengan huruf yang sama, sehingga lambang kimia bisa terdiri atas dua huruf. Hanya huruf pertama yang berupa huruf kapital.
Sehingga, helium ditulis ”He”, sedangkan barium ditulis ”Ba”. Besi mempunyi lambang kimia Fe yang berasal dari nama Latinnya ferrum.
Sebuah Unsur dengan Nama Lain
Untuk memutuskan nama suatu unsur merupakan suatu tantangan bagi para ilmuwan sepanjang abad. Di antara unsur-unsur yang telah dikenal luas, hampir semua negara memiliki nama unsurnya sendiri seperti emas, perak, atau raksa.
Sebagai contoh, Prancis dan Yunani menyebut nitrogen azote dan Jerman memakai kata Sauerstoff untuk oksigen. Sebagian menggunakan versi nama Latinnya yang mirip dengan nama setempatnya. Bahasa Latin untuk perak adalah argentum yang diubah menjadi argento dalam bahasa Italia dan argent dalam bahasa Prancis.
Untuk menghindari kebingungan dalam perdagangan internasional dan memastikan bahwa para ilmuwan seluruh negara dapat membahas unsur yang sama tanpa adanya risiko kesalahan dalam mencirikan nama-nama unsur telah dibakukan.
Badan yang mengawasi proses ini adalah International Union of Pure and Applied Chemistry atau IUPAC. Putusan tersebut antara lain bahwa secara internasional aluminium dan sesium harus dieja dengan ejaan Inggrisnya ”aluminium” dan “caesium” tetapi sulfur (belerang) harus menggunakan ejaan Amerika (bukan sulphur).
IUPAC juga terlibat dalam proses penamaan unsur-unsur baru yang masih sedang disintesis. Sering, unsur baru tersebut ditemukan oleh dua atau beberapa laboratorium dan mereka mungkin memiliki pendapat yang berbeda dalam hal penamaan.
Telah terjadi banyak perbedaan pendapat dalam pemberian nama unsur-unsur berat yang bernomor atom antara 104 dan 111.
Sekarang sudah disetujui sebagai rutherfordium (104), dubnium (105), seaborgium (106), bohrium (107), hassium (108), meitnerium (109), darmstadtium (110), dan roentgenium (111).
Unsur-unsur diluar unsur-unsur ini diberi nama menurut nomor-nomor atomnya dalam bahasa Latin (ununbium (112), ununtrium (113), ununquadium (114), dan selanjutnya).
Hampir semua unsur dinamakan berdasarkan nama tempat atau nama orang. Nama tempat biasanya merupakan tempat pertama kali unsur tersebut ditemukan atau negara penemunya.
Nama orang yang diambil untuk menghormati para ilmuwan terkenal atau tokoh-tokoh mitologi. Beberapa diberi nama berdasarkan benda-benda langit.
Unsur-unsur yang dinamakan berdasarkan nama tempat antara lain:
- Amerisium–Amerika
- Kalifornium–Negara bagian California Darmstadtium–Darmstadt, Jerman
- Europium–Eropa Fransium–Prancis
- Hafnium–Hafnia nama latin untuk Kopenhagen
- Holmium–Holmia nama latin untuk Stockholm
- Lutesium–Lutetia nama Latin untuk Prancis
- Magnesium–Magnesia, Yunani
- Polonium–Polandia
- Strontium–Strontian, Skotlandia
- Iterbium, Itrium–Iterbi, Swedia
Nama-nama unsur berdasarkan nama orang atau dewa antara lain:
- Bohrium–Niels Bohr
- Kurium–Pierre dan Marie Curie
- Einsteinium–Albert Einstein
- Fermium–Enrico Fermi
- Helium–Helios, Dewa Matahari Yunani Mendelevium–Dmitri Mendeleyev
- Niobium–Niobe, seorang wanita dalam mitologi Yunani Nobelium–Alfred Nobel
- Selenium–Selene, Dewi Bulan Yunani
- Torium–Thor, Dewa petir Skandinavia
- Telurium–Tellus, nama Latin untuk Bumi Vanadium–Vanadis, seorang dewi dari Skandinavia
Sifat-Sifat pada Tabel Periodik Unsur
Sekarang, tabel periodik terdiri atas 116 unsur yang tersusun dalam tujuh periode dan 18 golongan. Pada kondisi baku (suhu dan tekanan kamar), dua unsur berupa cairan (bromin dan merkurium), 11 berupa gas, dan sisanya padat.
Selain hidrogen dan merkurium, gas dan cairan terletak di sebelah kanan tabel. Hampir semua logam terletak di sisi kiri dan bawah tabel. Metaloid membentuk garis diagonal dari boron sampai telurium di sisi kanan tabel. Hampir semua nonlogam, seperti karbon, oksigen, nitrogen, dan halogen terletak di kanan dan atas tabel (di samping gas-gas mulia).
Jadi, ada kecenderungan umum bahwa sifat kelogaman unsur menjadi berkurang ketika melintasi periode dari kiri ke kanan.
Logam-logam alkali di Golongan 1 merupakan logam-logam lunak dengan titih leleh yang rendah. Logam-logam alkali tanah di Golongan 2 lebih keras dan mempunyai titik leleh yang lebih tinggi daripada logam-logam di Golongan 1.
Secara berangsur-angsur melintasi periode dari kiri ke kanan, unsur-unsur menjadi lebih keras dan memiliki titik leleh dan titik didih yang lebih tinggi. Sifat-sifat ini mencapai puncaknya di tengah-tengah tabel, lalu kekerasan, titik leleh, dan titik didih menurun kembali.
Pada kebanyakan versi tabel periodik, dua baris yang masing-masing berisi 14 unsur dapat ditemukan pada bagian bawah tabel. Empat belas unsur yang terletak di baris pertama disebut unsur lantanida dan baris kedua disebut unsur aktinida. Pemisahan kedua baris itu adalah untuk alasan kepraktisan.
Satu periode yang berisi 32 unsur sangat panjang untuk disusun dalam satu halaman buku berukuran normal. Namun, kebanyakan kimiawan setuju bahwa unsur-unsur lantanida dan aktinida memiliki cukup kesamaan untuk membentuk satu golongan terpisah yang disebut logam tanah langka.